Novo Nordisk nya trippelagonist visar bättre resultat än Retatrutid (19.7% vs 17.5%)
Läkemedel för behandling av obesitas har ökat kraftigt de senaste åren, både vad gäller användning och utveckling. De två preparat som i dag dominerar marknaden är semaglutid (Ozempic, Wegovy) och tirzepatid (Mounjaro).
Semaglutid är en uniagonist, vilket innebär att den verkar via en enda receptor – den är en analog till GLP-1 (glukagonlik peptid-1). Tirzepatid är däremot en dubbelagonist som aktiverar både GLP-1- och GIP-receptorer.
Inom en snar framtid väntas ännu mer potenta behandlingar nå marknaden i form av trippelagonister. Dessa läkemedel är utformade för att samtidigt aktivera tre olika receptorer: GLP-1, GIP och glukagonreceptorn, med målet att uppnå större viktnedgång och bredare metabola effekter.
Eli Lilly ligger för närvarande längst fram i utvecklingen av trippelagonister med läkemedelskandidaten retatrutid. I kliniska studier har retatrutid visat en genomsnittlig viktnedgång på omkring 25 procent efter 48 veckors behandling och cirka 17–18 procent efter 24 veckor.
UBT251 är en långverkande, syntetisk peptid som fungerar som en trippelagonist på GLP-1-, GIP- och glukagonreceptorerna. Läkemedlet utvecklades ursprungligen av United Bio-Technology och licensierades i mars 2025 till Novo Nordisk för global utveckling utanför Kina.
Den kliniska hypotesen bakom ”triple agonists” är att kombinationen av:
- GLP-1 (aptit/energiintag, magsäckstömning, glukoskontroll),
- GIP (metabola effekter, potentiellt förstärkning av vikt- och glukoseffekter i kombination),
- Glukagon (energiförbrukning och fettoxidation – men kräver balans för att undvika hyperglykemi), kan ge större viktminskning och bredare kardiometabol profil än ren GLP-1, med en farmakologi som liknar andra ”triagonister” i klassen.
Klinisk effekt (vikt och metabola mått)
Studie 1. Fas 2 prövning för övervikt/fetma – 24 veckor: upp till 19,7% viktnedgång
Den 24 februari 2026 rapporterade Novo Nordisk topline-resultat från en randomiserad, dubbelblind, placebokontrollerad fas 2-studie i Kina på personer med övervikt eller obesitas.
Inklusionkriterier
- Population: 205 kinesiska patienter med obesitas (BMI ≥ 28) eller övervikt (24 ≤ BMI < 28) med minst en viktrelaterad samsjuklighet.
- Medel vid baseline: kroppsvikt 92,2 kg, BMI 33,1 kg/m².
- Intervention: veckovis s.c. UBT251 2 mg, 4 mg, 6 mg vs placebo i 24 veckor.
- Primärt effektmått: procentuell förändring i kroppsvikt vid vecka 24.
Viktresultat
- Största observerade genomsnittliga viktminskningen: −19,7% (≈ −17,5 kg) vid vecka 24 i UBT251-arm (högsta effekt som observerades), jämfört med −2,0% (≈ −1,6 kg) med placebo.
Sekundära effektmått
- Novo Nordisk anger statistiskt signifikanta förbättringar vs placebo för ”key secondary endpoints” inklusive midjeomfång, blodglukos, blodtryck och lipider i alla dosgrupper. Exakta värden och p-värden är inte publicerade i pressmaterialet.
Vilka sekundära mått som är fördefinierade i studieregistrering:
I den registrerade studien listas bl.a. midjeomfång, BMI, faste-lipider, systoliskt/diastoliskt blodtryck, HbA1c, samt säkerhets- och PK/antikroppsmått (mer om detta nedan).
Viktigt: United Biotechnology har sagt att detaljerade data från den kinesiska fas 2-studien ska presenteras på en medicinsk kongress senare under 2026.
Studie 2. Fas 1 prövning för övervikt/fetma – 12 veckor: −15,1% i högsta dosgruppen
I samband med licensaffären (24 mars 2025) publicerades data från en genomförd fas 1b i Kina.
Upplägg
- Design: randomiserad, dubbelblind, placebokontrollerad fas 1b (säkerhet/tolerabilitet + PK/PD).
- N: 36 patienter i tre dosregimer:
- 1 mg
- 1 mg → 3 mg
- 1 mg → 3 mg → 6 mgDos-titrering, 1 injektion/vecka i 12 veckor.
Viktresultat:
- I högsta dosgruppen (titrering upp till 6 mg) minskade vikten i snitt −15,1% bland dem som fullföljde, medan placebo i snitt ökade +1,5%.
Det är den enda öppet redovisade siffran från fas 1b i fritt tillgängligt material (inga detaljerade sekundära utfall rapporterade i pressunderlaget).
Säkerhet och tolerabilitet
Fas 2 (Kina, 24 veckor)
- UBT251 beskrivs ha en säker och väl tolererad profil som är ”consistent with incretin-based therapies”.
- Vanligaste biverkningarna: gastrointestinala.
- Allvarlighetsgrad: ”vast majority” milda till måttliga och avtog över tid.
Notera: inga publika siffror anges i pressmaterialet för t.ex. illamående/kräkningar/diarré, avbrott p.g.a. biverkan, SAE, gallblåsa/pankreas-händelser osv. Sådant kan komma i kongresspresentationen.
Fas 1b (Kina, 12 veckor)
- Säkerhetsprofilen uppges vara i linje med inkretinbehandlingar.
- GI-biverkningar var vanligast och i stor majoritet milda–måttliga.
Utvecklingsstatus och kommande datapunkter
- Novo Nordisk uppger att de har startat en global fas 1b/2a-studie i cirka 330 personer med övervikt/fetma, med upp till 28 veckors behandling; topline väntas 2027.
- Novo Nordisk förväntar sig också att initiera en fas 2-studie i typ 2-diabetes under andra halvåret 2026.
- Novo Nordisk listar UBT251 i sin publika R&D pipeline som en ”GGG tri-agonist”.
Är UBT251 bättre än Retatrutide?
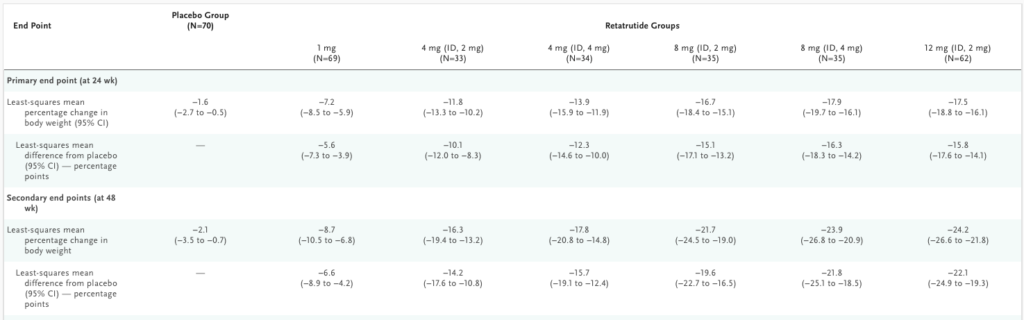
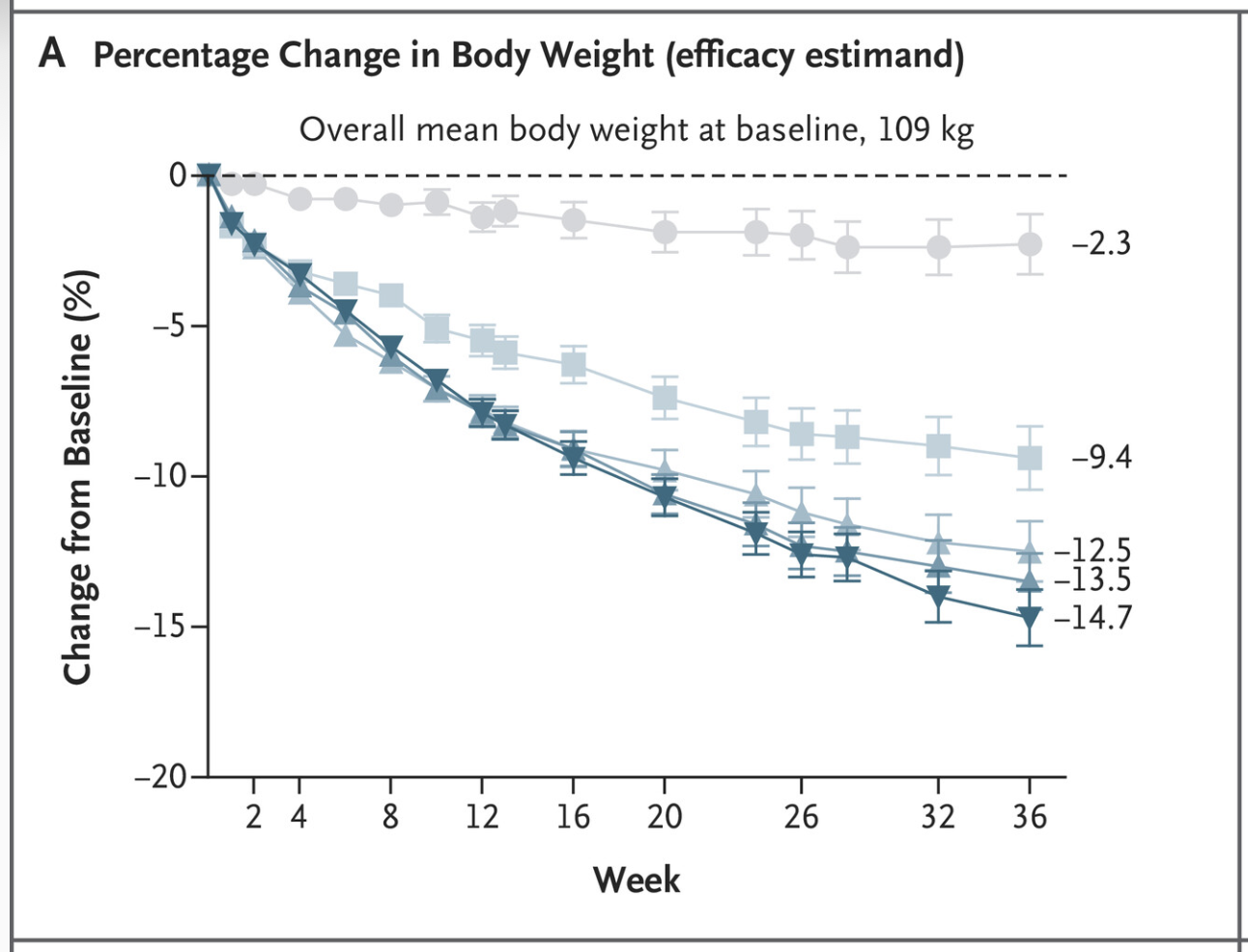
Retatrutid har studerats i flera kliniska prövningar och har visat en mycket kraftig viktnedgång – i vissa studier upp till närmare 30 procent efter drygt ett års behandling. Figuren nedan är hämtad från www.metdis.org, en hemsida som sammanställer data om läkemedel inom metabolism, obesitas och diabetes. Resultaten illustrerar viktnedgångseffekten av retatrutid, som är Eli Lillys hittills mest potenta läkemedelskandidat för viktbehandling. Preparatet är dock ännu inte godkänt och finns därför inte tillgängligt på marknaden.
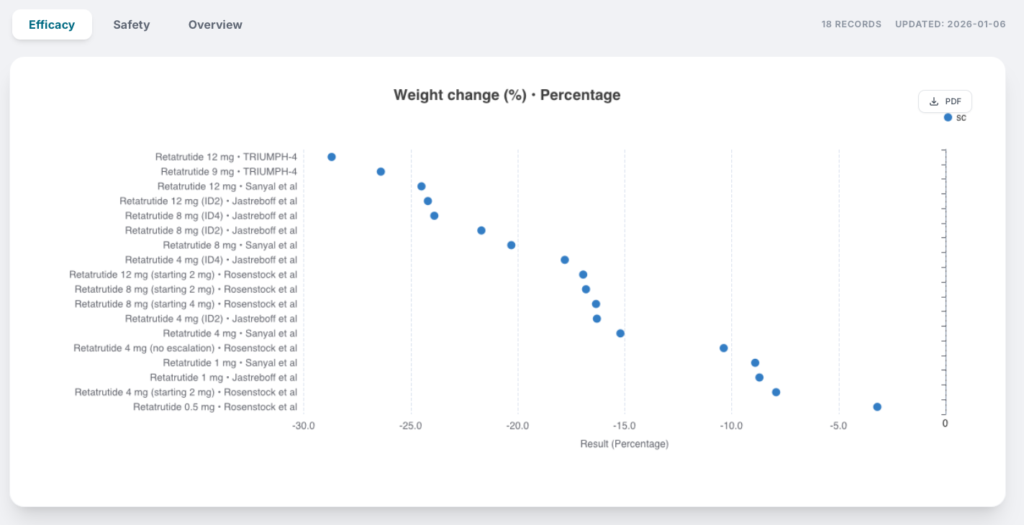
Resultaten i figuren ovan visar effekten vid studiens slutpunkt. Eftersom UBT251 hittills endast har följts under 24 veckor är det mest relevant att jämföra resultaten med retatrutid vid samma tidpunkt.
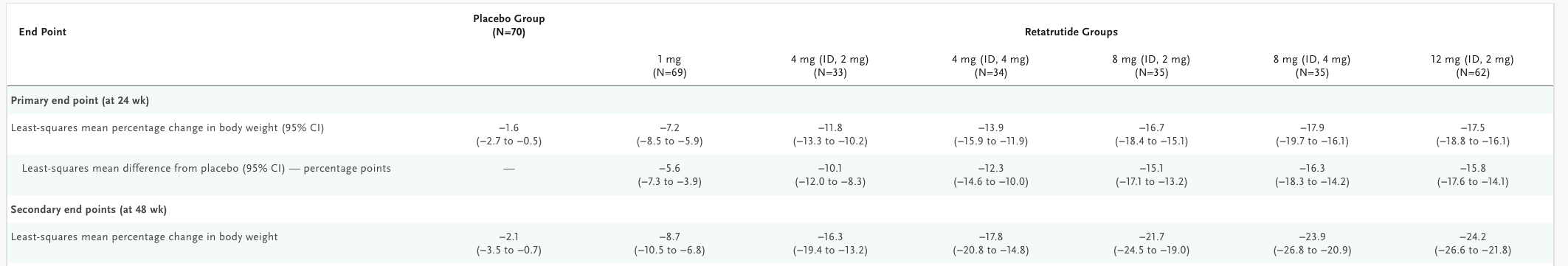
Tabellen nedan visar att den högsta studerade dosen av retatrutid (12 mg) resulterade i en genomsnittlig viktnedgång på 17,5 procent efter 24 veckor, medan UBT251 uppnådde 19,7 procent under motsvarande tidsperiod.
Novo Nordisk har ännu inte inlett en fas 3-studie med UBT251 och den högsta möjliga dosnivån har inte heller fastställts. Det innebär att den slutliga kliniska dosen potentiellt skulle kunna ge ännu bättre effekt, förutsatt att säkerhetsprofilen förblir gynnsam och att biverkningarna inte ökar.